 |
| Źródło: Wikipedia. Mitochondrialny cytochrom bc1. |
1) Cytochrom b/b6 - jest to główna podjednostka transbłonowych kompleksów cytochromów bc1 i b6f. Cytochrom b jest jedną z trzech podjednostek katalitycznych (obok cytochromu c1 i białka Rieskiego), występującej w mitochondriach eukariotów i bakteriach tlenowych, oksydoreduktazy ubichinol-cytochrom c, występującej również pod nazwami kompleks III lub cytochromu bc1 - w zależności od organizmu. Podobną funkcję w chloroplastach roślin i sinic pełni analog cytochromu b - cytochrom b6, który jest częścią kompleksu cytochrom b6f.
2) Cytochrom f- jest to największa podjednostka kompleksu cytochromów b6f (reduktaza plastochinol - plastocyjanina; o masie 19 kDa. Cytochrom f znajduje się po wewnętrznej stronie błony tylakoidu a część cytochromu wystająca z błony jest miejscem wiązania ruchliwego przenośnika elektronów - plastocyjaniny. Hem jest związany pomiędzy dwoma krótkimi helisami w N-końcu cytochromu f. Druga helisa posiada sekwencje zbliżoną do cytochromu c, Cys-Xaa-Xaa-Cys-His, która jest związana kowalencyjnie z cząsteczką hemu wiązaniem tioestrowym dwóch reszt cysteinowych. Piąty atom żelaza hemu połączony jest przez histydynę a szósty przez grupę alfa-aminową tyrozyny z N-końca polipeptydu. Cytochrom f posiada wewnętrzną sieć cząsteczek wody. Przypuszcza się, że sieć ta może służyć do przenoszenia protonów.
3) Feofityna - jest to organiczny związek chemiczny o oliwkowo-brunatnej barwie, będący cząsteczką chlorofilu, w którym atom magnezu został zastąpiony przez dwa atomy wodoru. Związek ten można uzyskać poprzez działanie kwasem na chlorofil. Feofityna jest naturalnie obecna w częściach zielonych roślin, gdzie bierze udział w przenoszeniu elektronów w fazie jasnej fotosyntezy.

Źródło: Wikipedia. Feofityna a.
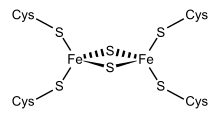 |
| Źródło: Wikipedia. Centrum 2Fe-2S. |
4) Ferredoksyna, Fd - białko stromy chloroplastów o masie 12 kDa, zawierające grupę prostetyczna 2Fe-2S. Może występować w formie zredukowanej Fdred lub utlenionej Fdutl. Kodowane w jądrze komórkowym w formie prebiałka znakowanego N-końcowym peptydem tranzytowym, który jest odcinany przez stromalną peptydazę procesową w stromie. Tu również jest przyłączane centrum 2Fe-2S. Jest jednym z białek łańcucha fotosyntetycznego transportu elektronów - przenosi elektrony z fotosystemu I do reduktazy ferredoksyna-NADP. Ponadto może brać udział w cyklicznym transporcie elektronów oraz pełnić funkcję reduktaz: azotynowej, siarczynowej, ferredoksyno-tioredoksyny oraz syntetazy glutaminowej. Istnieją również bakteryjne ferredoksyny zawierające inne centra żelazo-siarkowe: 4Fe-4S i 3Fe-4S.
5) Kompleks cytochromów b6f, plastochinol - plastocyjanina reduktaza - jest to białko obecne w błonach tylakoidów, chloroplastów eukariontów i błonach tylakoidów sinic. Kompleks bierze udział w przenoszeniu elektronów z fotoukładu II na fotoukład I. Przenoszeniu elektronów towarzyszy przemieszczenie protonów ze stromy do wnętrza tylakoidów, czyli generowanie gradientu elektrochemicznego, w tak zwanym cyklu Q, niezbędnego wytworzenia energii użytecznej metabolicznie w postaci ATP. Kompleks jest homodimerem o masie całkowitej 220 kDa. Każdy z monomerów składa się z czterech podjednostek. Pierwsza z nich to cytochrom b6, będący integralnym białkiem błonowym o masie 24 kDa. Białko składa się z czterech wewnętrznych podjednostek i dwóch cząsteczek hemu typu b. Jedna z cząsteczek hemu znajduje się po stromalnej części i jest określana jako hem wysokopotencjałowy, a druga po stronie wnętrza tylakoidu - hem niskopotencjałowy. Podjednostka IV o masie 17 kDa jest integralnym białkiem błonowym, umożliwiającym przyłączenie do każdego z monomerów po jednej cząsteczce chlorofilu i beta-karotenu. Funkcja przyłączanych barwników nie jest znana. Przyłączone cząsteczki mogą stabilizować kompleks lub brać udział w regulacji aktywności kinazy LHC (kompleksy zbierające energię świetlną), z cytochromu b elektrony przekazywane są na cytochrom f za pośrednictwem białka Rieskiego o masie 17,5 kDa, zawierającego centra żelazo-siarkowe [2Fe-2S]. Cytochrom f zawierający jedną cząsteczkę hemu ma masę 19 kDa i jest miejscem wiązania plastocyjaniny odbierającej elektrony z kompleksu cytochromów. Struktura i funkcje kompleksu cytochromów b6f są zbliżone do kompleksu cytochromów bc1 obecnego w mitochondriach i błonach fotosyntetyzujących bakterii purpurowych.
Jakkolwiek są ważne różnice między dwoma kompleksami: Cytochrom pojedynczego polipeptydu b w kompleksie cytochromów bc1 odpowiada cytochromowi b6 i podziałowi IV w cytochrom b6f złożonym; Cytochrom f nie jest homologiczny z cytochromem c1; Kompleks cytochromów b6f zawiera dodatkowe cząsteczki barwników, chlorofil, beta-karoten oraz hem c połączony przez pojedyncze wiązanie tioestrowe z cytochromem b6.
 |
| Źródło: Wikipedia. |
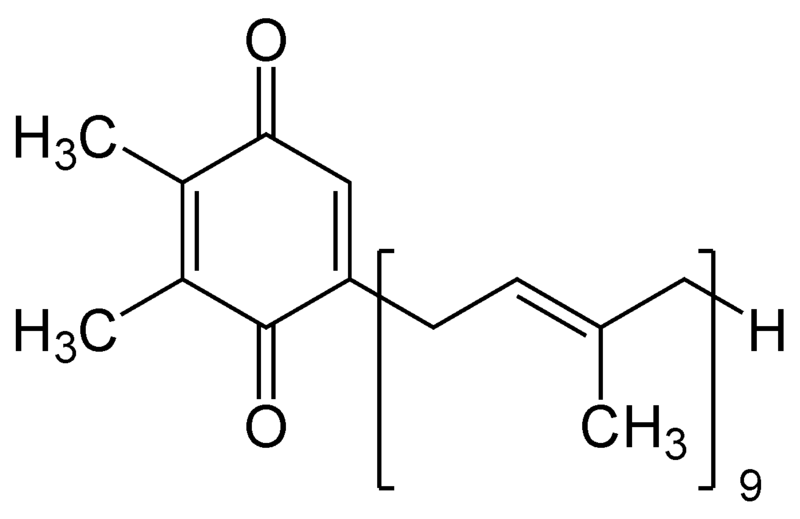 |
| Źródło: WIkipedia. Plastochinon. |
6) Plastochinon - jest to organiczny związek chemiczny z grupy chinonów, występujący w chloroplastach komórek roślinnych. Jest odpowiedzialny za przenoszenie elektronów w fazie jasnej fotosyntezy. Przenosi elektrony z centrum reakcji fotosystemu II na kompleks cytochromowy b6f. Po przyłączeniu dwóch elektronów i dwóch protonów pobranych ze stromy chloroplastów plastochinon przechodzi w formę zredukowaną - plastochinol - PQH2.
BUDOWA: Nazwą plastochinon określa się grupę związków różniących się długośćią bocznego łańcucha izoprenoidowego od 6 do 10 jednostek izoprenoidowych. Najczęstszą formą plastochinonu jest PQ-9.
7) Plastocyjanina (PCY z ang. plastocyanin) - jest niewielkim zawierającym miedź białkiem uczestniczącym w transporcie elektronów. U większości roślin naczyniowych białko jest monomerem o masie 10,500 Da i zbudowanym z 99 aminokwasów. U pozostałych organizmów przeprowadzających fotosyntezę może nieznacznie różnić się od tej formy. Białko występuje po wewnętrznej stronie błony tylakoidu.
 |
| Źródło: Wikipedia. Model budowy plastocyjaniny. |
ROLA BIAŁKA: W fazie jasnej fotosyntezy plastocyjanina przenosi elektron z cytochromu f wchodzącego w skład kompleksu cytochromowego b6f do centrum reakcji fotosystemu I. Atom miedzi obecny w plastocyjaninie w wyniku przyjęcia elektronu ulega redukcji zgodnie z równaniem: Cu2+Pc + e- -> Cu+Pc ; Podczas oddawania elektronu do centrum reakcji fotosystemu I zachodzi reakcja odwrotna.




Brak komentarzy:
Prześlij komentarz