 |
| Źródło: Wikipedia. Model budowy atomu Bohra. |
*Model budowy atomu wodoru Bohra – model atomu wodoru autorstwa Nielsa Bohra opracowany w 1913 roku[1]. Bohr przyjął wprowadzony przez Ernesta Rutherforda model atomu, według którego elektron krąży wokół jądra jako naładowany punkt materialny, przyciągany przez jądro siłami elektrycznymi.
Model atomu Rutherforda nie przewidywał dyskretnego charakteru widma promieniowania wysyłanego przez atomy oraz nie wyjaśniał ich stabilności. Niels Bohr usunął te trudność proponując model atomu oparty na dwóch nowych postulatach, sprzecznych z klasyczną elektrodynamiką. Dzięki temu jednak zdołał wyjaśnić pojawianie się linii widmowych gazowego wodoru oraz wyprowadził wzory, pozwalające teoretycznie obliczać długości fal promieniowania elektromagnetycznego emitowanego przez wodór.
Zastosowanie modelu Bohra nie ogranicza się jedynie do atomu wodoru. Model ten jest uniwersalny w tym sensie, że jest słuszny dla układu dwóch dowolnych cząstek naładowanych, które krążą wokół wspólnego środka masy z prędkościami znaczne mniejszymi od prędkości światła. Model ten jest więc poprawny dla układu jednoelektronowego takiego jak atom wodoru, ale też jest słuszny dla pojedynczo zjonizowanego atomu helu, podwójnie zjonizowanego atomu litu itd. Modelem tym można także opisać pozytonium (czyli układ elektron-pozyton) oraz stany Rydberga jakiegokolwiek atomu, tj. takie stany atomowe, w których jeden elektron jest w znacznej odległości od reszty atomu. Model ten może być także użyty do obliczania linii K promieniowania X, pod warunkiem, że doda się dodatkowe założenia (por. prawo Moseleya). W fizyce wysokich energii może być użyty do obliczania mas mezonów zbudowanych z ciężkich kwarków.
W modelu Bohra elektron krąży wokół jądra atomu po orbicie kołowej. Przez analogię do ruchu planet wokół Słońcamodel ten nazwano „modelem planetarnym atomu”.
Model ten nie wyjaśnia spinu elektronu, nie nadaje się do opisu atomów wieloelektronowych. Został zastąpiony przez dokładniejsze modele kwantowe (patrz niżej).
Postulaty Bohra z mechaniki klasycznej
Model Bohra jest modelem po części opartym na klasycznej elektrodynamice, zakładającym żeː
(P1) Elektron jest utrzymywany na orbicie kołowej za pomocą sił elektrycznego oddziaływania z jądrem. Siła dośrodkowa jest więc siłą Coulomba
gdzieː
- – masa elektronu,
- – prędkość elektronu,
- – promień orbity elektronu,
- – stała oddziaływań elektrycznych,
- – ładunek jądra (równy liczbie atomowej),
- – ładunek elektronu.
(P2) Całkowita energia elektronu w atomie jest sumą energii kinetycznej oraz energii potencjalnej oddziaływań elektrycznych
Powyższe równania zakładają, że masa jądra jest o wiele większa niż masa elektronu (co jest słuszne, gdyż np. masa protonu jest około 1830 razy większa niż masa elektronu).
Z rozwiązania układu tych równań otrzymuje się, iż energia całkowita jest równa energii kinetycznej ze znakiem minus
oraz
czyliː energia całkowita jest równa połowie energii potencjalnej; energia całkowita jest ujemna i jest odwrotnie proporcjonalna do Oznacza to, że trzeba dostarczyć elektronowi energii z zewnątrz, aby przenieść go dalej od protonu. Dla dążące do nieskończoności energia rośnie do zera. (Własność, iż całkowita energia jest połową energii potencjalnej jest na mocy twierdzenia o wiriale słuszna dla dowolnych orbit, niekoniecznie kołowych).
Postulaty kwantowe Bohra
O rewolucyjności podejścia Bohra decydują sformułowane przez niego zasady kwantowe. Postulaty te były wprowadzone ad hoc, aby uzyskać zgodność przewidywań modelu z eksperymentami.
(P3) Postulat o kwantyzacji orbitalnego momentu pędu elektronu. Z nieskończonej liczby orbit, które dopuszczałaby mechanika klasyczna, elektron może poruszać się tylko po tych, dla których moment pędu elektronu jest równy całkowitej wielokrotności stałej Plancka podzielonej tj.
gdzieː
- – stała Plancka podzielona przez
(P4) Postulat o promieniowaniu. Elektron poruszając się po danej orbicie nie emituje ani nie pochłania energii. Elektron emituje foton, jeżeli spada z orbity wyższej na niższą, a pochłania foton, jeżeli przechodzi z orbity niższej na wyższą; energia emitowanego(pochłanianego) fotonu jest równa różnicy między energią wyższą i niższą elektronu
gdzieː
- – energie elektronu, odpowiednio, wyższa i niższa,
- – stała Plancka,
- – częstotliwość fotonu.
Kwantowanie promieni orbit oraz energii
Z postulatu kwantowania momentu pędu wynika, iż promienie orbit oraz energia są skwantowane, tj. mogą przyjmować tylko dyskretne wartości.
Aby to pokazać zauważmy, że pierwsze równanie implikuje zależność prędkości od promienia
Wstawiając tę zależność do wzoru na kwantowanie momentu pędu otrzyma się równanie zależne tylko od stąd dostaje się dozwolone promienie orbit
Widać, że promienie orbit rosną proporcjonalnie do kwadratu numeru orbity.
Najmniejsza możliwa wartość promienia orbity w atomie wodoru () jest nazywana promieniem Bohra i wynosi
Dowolny promień orbity można więc wyrazić w zależności od liczby kwantowej oraz
Ponieważ energia zależy
więc ostatecznie otrzymamy, iż energia -tego poziomu jest odwrotnie proporcjonalna do kwadratu liczby kwantowej oraz energii
gdzie – energia stanu podstawowego atomu
Podsumowanie
Z postulatu (P3) o kwantowaniu momentu pędu wynika, że promienie orbit elektronu oraz energie elektronu w atomie są również skwantowane. Promienie te, w szczególności promień atomu wodoru w stanie podstawowym (tzw. promień atomu Bohra) oraz energie można wyznaczyć zakładając, iż elektron podlega prawu klasycznego oddziaływania elektrycznego klasycznego (postulaty (P1) oraz (P2)).
Postulat kwantowy (P4) o promieniowaniu atomu zakłada, że elektron krążąc po określonej orbicie nie emituje promieniowania, wbrew prawu promieniowania klasycznej elektrodynamiki (głoszącemu, iż cząstka naładowana krążąc po orbicie powinna emitować promieniowanie elektromagnetyczne i tracić energię), ale promieniowanie jest emitowane tylko wówczas, gdy elektron zmienia orbitę. Zgodnie z elektrodynamiką klasyczną elektron poruszając się ruchem niejednostajnym wokół jadra powinien promieniować energię w postaci fali elektromagnetycznej, w wyniku czego musiałby „spaść” na jądro już po czasie rzędu 10−6 sekundy i atom przestałby istnieć.
Model Bohra, jakkolwiek będący sztucznym połączeniem mechaniki klasycznej i nowych postulatów kwantowych, daje prawidłowe wyniki dotyczące wartości energii elektronu w atomie wodoru oraz długości fal emitowanych przez wodór (linie widmowe wodoru). Jest też poprawny w odniesieniu do tzw. atomów wodoropodobnych, tj. atomów zjonizowanych tak, że posiadają tylko jeden elektron.
Mimo ogromnego sukcesu modelu, za który Bohr otrzymał w 1922 r. nagrodę Nobla w dziedzinie fizyki, model ten pozostawiał wiele nie rozwiązanych problemów. M.in. nie dało się go zaadaptować do opisu atomów posiadających więcej niż dwa elektrony. Nie można też było za jego pomocą stworzyć zgodnej ze faktami eksperymentalnymi teorii wiązań chemicznych. Także wielkim problemem był fakt, iż model łączył w sobie sprzeczne idee, tj. zakładał postulaty kwantowe sprzeczne z prawami klasycznej elektrodynamiki, mimo iż częściowo na nich opierał się.
Zastąpienie modelu Bohra przez modele kwantowe
Kolejne, lepsze modele atomu wodoru oraz atomów wieloelektronowych zostały dostarczone przez mechanikę kwantową(równanie Schrödingera 1926 r., równanie Pauliego 1927 r., równanie Diraca 1928 r.) oraz elektrodynamikę kwantową. Modele te pozwalały z coraz lepszą precyzją obliczać długości linii widmowych atomów i cząsteczek odpowiadającą coraz bardziej precyzyjnym pomiarom (np. pomiar przesunięcia Lamba) czy obliczać moment magnetyczny elektronu. Dzięki temu wytłumaczono też spin elektronu i wiązania chemiczne.
 Michał Gryziński (ur. 29 września 1930 w Warszawie, zm. 1 czerwca 2004) – polski fizyk jądrowy, specjalista z zakresu fizyki plazmy i twórca kontrowersyjnego modelu budowy atomu, znanego jako model Gryzińskiego.
Michał Gryziński (ur. 29 września 1930 w Warszawie, zm. 1 czerwca 2004) – polski fizyk jądrowy, specjalista z zakresu fizyki plazmy i twórca kontrowersyjnego modelu budowy atomu, znanego jako model Gryzińskiego.Życiorys
Uzyskał tytuł magistra inżyniera na Wydziale Łączności Politechniki Warszawskiej w 1955 oraz doktorat z fizyki teoretycznej w Instytucie Badań Jądrowych w 1966. Zajmował się teorią zderzeń atomowych i budową atomu, astrofizyką, fizyką plazmy i kontrolowaną syntezą termojądrową.
Michał Gryziński był z zamiłowania turystą, przebywał m.in. w Nepalu, na Ałtajui Kaukazie. Był także zapalonym sportowcem – uprawiał siatkówkę, pływanie, wioślarstwo, żeglarstwo i narciarstwo.
Źródło informacji: ftj.agh.edu.pl
*Struktura molekularna i molekularny orbital wodoru cząsteczkowego:
Źródło: http://hyperphysics.phy-astr.gsu.edu/hbase/molecule/hmol.html#c1
Źródło: http://www.nyu.edu/classes/tuckerman/adv.chem/lectures/lecture_13/node3.html
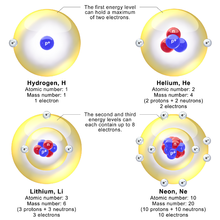
*Wodór (H, łac. hydrogenium) - jest to pierwiastek chemiczny o liczbie atomowej 1, niemetal z bloku s układu okresowego. Wodór jest najczęściej występującym pierwiastkiem chemicznym we Wszechświecie i jednym z najczęściej spotykanych pierwiastków na Ziemi. Posiada najmniejszą masę atomową, wynoszącą 1,00794 u. Najczęściej występującym izotopem wodoru jest prot (1H), który posiada atom o najprostszej możliwej budowie – składa się z jednego protonu i jednego elektronu.
Wodór w formie atomowej powstał w epoce rekombinacji. W warunkach standardowych, wodór gazowy występuje w formie cząsteczkowej H2, jako bezbarwny, bezwonny, bezsmakowy, nietoksyczny, łatwopalny gaz. W skrajnie wysokich temperaturach możliwe jest jego uzyskanie w formie atomowej H. Ponieważ pierwiastek ten łatwo tworzy związki chemiczne z większością pierwiastków będących niemetalami, większość wodoru na Ziemi występuje w postaci wody lub związków organicznych. Wodór odgrywa szczególnie istotną rolę w reakcjach kwasowo-zasadowych, ponieważ większość tego typu reakcji wiąże się z wymianą protonów między rozpuszczalnymi cząsteczkami. W związkach jonowych wodór może posiadać ładunek ujemny (anion H-) lub dodatni (kation H+). Ponieważ wodór jest jedynym neutralnym atomem, dla którego równanie Schrödingera można rozwiązać analitycznie, badania energetyki i wiązań wodoru odegrały kluczową rolę w rozwoju mechaniki kwantowej.
Wodór po raz pierwszy otrzymano sztucznie na początku XVI wieku w reakcji metalu z kwasem. W latach 1766–81 Henry Cavendish był pierwszą osobą, która stwierdziła, że wodór jest oddzielną substancją chemiczną, po spaleniu której powstaje woda. Właściwość ta zadecydowała o nazwie tego pierwiastka chemicznego, bowiem w języku greckim υδρογόνο (ydrogóno) oznacza „tworzący wodę”.
Produkcja przemysłowa wodoru odbywa się głównie metodą reformingu parowego gazu ziemnego, rzadziej zaś przy użyciu bardziej energochłonnych metod, takich jak elektroliza wody. Zdecydowana większość otrzymanej w ten sposób substancji spożytkowywana jest w okolicach miejsca produkcji. Dwa największe obszary zastosowań tak otrzymanego wodoru to przetwarzanie paliw kopalnych (np. hydrokraking) i produkcja amoniaku, głównie do zastosowania na rynku nawozowym.
Pochodzenie i występowanie: Stanowiąc około 75% (masowo) całości materii, wodór jest najpowszechniej występującym pierwiastkiem we Wszechświecie. Zgodnie z teorią Wielkiego Wybuchu, wodór jest pierwiastkiem powstałym w bardzo wczesnym etapie rozwoju Wszechświata (podczas Wielkiego Wybuchu powstała także większość jąder helu oraz część istniejących obecnie jąder litu i berylu). Początkowo materia Wszechświata składała się z promieniowania i cząstek o bardzo wysokiej energii (w tym z fotonów, elektronów, protonów, neutronów, cząstek neutrino oraz antycząstek). W miarę wychładzania się materii, w czasie około stu sekund od początku Wielkiego Wybuchu, temperatura spadła do miliarda stopni Celsjusza. W takiej temperaturze energia cząstek była już zbyt mała, aby pokonać siłę międzyatomowego oddziaływania silnego, skutkiem czego byłą łączenie się protonów i neutronów w deuter (ciężki atom wodoru, zawierający jeden proton i jeden neutron), atom helu (zawierający dwa protony i dwa neutrony) oraz małe ilości atomów litu i berylu. Większość protonów utworzyła natomiast atomy zwykłego wodoru.
W dużych ilościach wodór można znaleźć np. w gwiazdach (w tym w Słońcu), materii międzygwiazdowej oraz w przestrzeni międzyplanetarnej.
Chmury wodorowe (mgławice o gęstym nagromadzeniu wodoru cząsteczkowego H2, zwane obszarami H II) są miejscem narodzin nowych gwiazd. Posiadając zwiększoną gęstość, chmury wodorowe dają początek procesowi tworzenia się gwiazd.
Pochodzenie i występowanie: Stanowiąc około 75% (masowo) całości materii, wodór jest najpowszechniej występującym pierwiastkiem we Wszechświecie. Zgodnie z teorią Wielkiego Wybuchu, wodór jest pierwiastkiem powstałym w bardzo wczesnym etapie rozwoju Wszechświata (podczas Wielkiego Wybuchu powstała także większość jąder helu oraz część istniejących obecnie jąder litu i berylu). Początkowo materia Wszechświata składała się z promieniowania i cząstek o bardzo wysokiej energii (w tym z fotonów, elektronów, protonów, neutronów, cząstek neutrino oraz antycząstek). W miarę wychładzania się materii, w czasie około stu sekund od początku Wielkiego Wybuchu, temperatura spadła do miliarda stopni Celsjusza. W takiej temperaturze energia cząstek była już zbyt mała, aby pokonać siłę międzyatomowego oddziaływania silnego, skutkiem czego byłą łączenie się protonów i neutronów w deuter (ciężki atom wodoru, zawierający jeden proton i jeden neutron), atom helu (zawierający dwa protony i dwa neutrony) oraz małe ilości atomów litu i berylu. Większość protonów utworzyła natomiast atomy zwykłego wodoru.
W dużych ilościach wodór można znaleźć np. w gwiazdach (w tym w Słońcu), materii międzygwiazdowej oraz w przestrzeni międzyplanetarnej.
Chmury wodorowe (mgławice o gęstym nagromadzeniu wodoru cząsteczkowego H2, zwane obszarami H II) są miejscem narodzin nowych gwiazd. Posiadając zwiększoną gęstość, chmury wodorowe dają początek procesowi tworzenia się gwiazd.
Niedawne obserwacje wykazały, że ogólnie rzecz biorąc, bardzo niewielka liczba rejonów H II znajduje się poza obrębem galaktyk. Takie międzygalaktyczne obszary H II są prawdopodobnie pozostałościami mniejszych galaktyk rozerwanych przez siły pływów grawitacyjnych[11].
Morfologia
Obszary H II występują w ogromnej różnorodności rozmiarów. Każda gwiazda w regionie H II jonizuje z grubsza sferyczny obszar otaczający ją, zwany strefą Strömgrena, lecz połączenie bąbli jonizacji wielokrotnych układów gwiazdowych w rejonie H II oraz ekspansji podgrzanych mgławic w otaczające gazy o ostrych gradientach gęstości daje w wyniku skomplikowane kształty. Wybuchy supernowych także wpływają na kształt obszarów H II. W pewnych przypadkach, powstawanie dużych gromad gwiazdowych w regionie H II daje w rezultacie obszary wyglądające na wydrążone od środka. Tak jest w przypadku NGC 604, olbrzymiego obszaru H II w galaktyce Trójkąta.
Godne uwagi rejony H II
W naszej Galaktyce, najlepiej znanym obszarem H II jest Mgławica Oriona, która leży 1500 lat świetlnych stąd. Mgławica Oriona jest częścią ogromnego obłoku molekularnego, który wypełniłby większą część gwiazdozbioru Oriona, gdyby był widzialny. Mgławica Koński Łeb i Pętla Barnarda to dwie inne oświetlone części tej chmury gazu.
Wielki Obłok Magellana, galaktyka satelitarna Drogi Mlecznej, zawiera ogromny obszar H II zwany Mgławicą Tarantula. Ta mgławica jest znacznie większa niż mgławica Oriona i tworzy tysiące gwiazd; niektóre z nich posiadają masę ponad 100 mas Słońca. Gdyby mgławica Tarantula była tak blisko Ziemi, jak mgławica Oriona, świeciłaby w przybliżeniu tak jasno jak Księżyc w pełni na nocnym niebie. Supernowa SN 1987A wybuchła na obrzeżu mgławicy Tarantula.
Mgławica NGC 604 jest jeszcze większa niż mgławica Tarantula, ma rozmiary rzędu 1300 lat świetlnych, chociaż zawiera mniejszą liczbę gwiazd. Jest to jeden z największych obszarów H II w Grupie Lokalnej.
Łuk Rysia to najgorętszy, najmasywniejszy i najodleglejszy od Słońca rejon gwiazdotwórczy, jaki odkryto w widzialnym Wszechświecie[12].
Aktualne kwestie w badaniach nad rejonami H II
Podobnie jak w przypadku mgławic planetarnych, określenie składu pierwiastkowego w obszarach H II jest niepewne. Istnieją dwie różne metody wyznaczenia ilości metali (tj. pierwiastków cięższych niż wodór i hel) w mgławicach, opierające się na analizie typów linii widmowych. Różnice pomiędzy wynikami obu metod wprowadzają często duże rozbieżności. Niektórzy[kto?] astronomowie przypisują je obecności niewielkich fluktuacji temperatur wewnątrz obszarów H II. Według innych rozbieżności są zbyt duże, aby wyjaśnić je efektem temperaturowym. Prowadzi to do hipotezy głoszącej, że obserwowane różnice da się wyjaśnić istnieniem zimnych skupisk zawierających niewielkie ilości wodoru[13].
Pełne szczegóły masywnego powstawania gwiazd w obszarach H II nie są do tej pory dobrze poznane. Dwa główne problemy utrudniają badania na tym polu. Pierwszy, to znacząca odległość dużych obszarów H II od Ziemi, przy czym najbliższy rejon H II znajduje się ponad 1000 lat świetlnych stąd, a inne są położone w odległości kilka razy większej. Po drugie, powstawanie gwiazd jest silnie przesłonięte przez pył i obserwacje w świetle widzialnym są niemożliwe. Fale radiowe i światło podczerwone mogą przenikać pył, ale najmłodsze gwiazdy mogą nie emitować wystarczającej ilości energii w tych zakresach długości fali.
-------------------
(...) Wodór jest trzecim pod względem częstości występowania pierwiastkiem na Ziemi (głównie w cząsteczkach wody oraz węglowodorów). Wynika to z małej masy, która powoduje powolne ulatywanie wodoru cząsteczkowego z atmosfery w przestrzeń kosmiczną.
Wodór na Ziemi występuje np. w:
- skałach (np. granicie – 61,68%; gabro – 88,42%; gnejsie – 61,93%; bazalcie - 36,15%; piroksenach – 12,49%);
- złożach gazu ziemnego (składającego się głównie z metanu), którego bogate złoża znajdują się m.in. w Iranie, Katarze czy Rosji;
- gazach wulkanicznych;
- powietrzu – w śladowych ilościach ok. 0,019%.
Historia i etymologia: Pierwsze obserwacje wodoru przypisuje się szwajcarskiemu alchemikowi Paracelsusowi. Wykonywał on eksperymenty polegające na wrzucaniu metali do kwasów i zbieraniu do naczyń gazowych produktów tych reakcji. W swoim dziele Archidoxa odnotował on, że powietrze powstałe w wyniku połączenia żelaza i rozcieńczonego kwasu solnego "unosi się i wybucha jak wiatr" (Lufft sich erhebt und herfür bricht gleich wie ein Wind). Niejednoznaczność opisu powstałego zjawiska sprawia, że nie jest do końca jasne, czy gazem, który zaobserwował, był rzeczywiście wodór czy powstające pęcherzyki powietrza. Do dzisiaj reakcja metali z kwasami stanowi najprostszy sposób otrzymywania wodoru w warunkach laboratoryjnych.
W 1671 roku Robert Boyle opublikował Tracts containing new experiments touching the relation betwixt flame and air, w którym opisał wybuchową naturę mieszanki wodoru z powietrzem, powstałej w wyniku reakcji opiłków żelaza z kwasami, nazywając ją Inflammable solution of Mars(łatwopalnym roztworem Marsa).
 |
| Źródło: Wikipedia. Antoine Lavoisier. |
Pierwszą osobą, która uznała wodór za odrębną substancję (flogiston) był Henry Cavendish. W 1766 r. zamieścił on w swoich notatkach wyniki i wnioski ze swoich badań. Substancja ta została uznana za pierwiastek dzięki badaniom Antoine'a Lavoisiera nad otrzymywaniem wody z wodoru i tlenu w 1783 r. Lavoisier nadał wodorowi nawę hydrogenium oznaczającą "rodzący wodę". Nazwa ta pochodzi z greckiego i jest połączeniem dwóch wyrazów „hydōr” (ὕδωρ) oznaczający „wodę” oraz „genes” (-γενής) oznaczający „tworzący”, „rodzący”. Nazwa ta rozprzestrzeniła się w Europie i do dzisiaj jej pochodne są używane w wielu językach. Przykładem jest angielskie słowo „hydrogen” lub francuskie „Hydrogène”.
 | |||||||||||||||
 ZastosowaniePrzemysł chemiczny
Wodór znajduje szerokie zastosowanie w przemyśle chemicznym oraz petrochemicznym. Wykorzystywany jest głównie w procesach redukcji i uwodornienia. Przykładami procesów, w których stosowany jest wodór są:






Wilhelm Normann (1870-1939) - niemiecki chemik. Wynalazł i opatentował metodę katalitycznego utwardzania (uwodorniania) tłuszczów. Jego odkrycie miało duże znaczenie w przemyśle spożywczym, między innymi w produkcji margaryny. Prace Normanna pozwoliły uzyskiwać tłuszcze typu trans.

Proces ten prowadzony jest w podwyższonej temperaturze i ciśnieniu. Polega on na przepuszczaniu wodoru przez ogrzany olej, który zawiera katalizator (najczęściej mrówczan niklu). Metoda ta, opracowana została w 1902 przez Wilhelma Normanna (1870-1939) i przyczyniła się do rozwoju przemysłu margarynowego oraz umożliwiła zastosowanie olejów roślinnych w procesie otrzymywania mydła.
 
Inną metodą utwardzania tłuszczów jest metoda Wilbuszewicza. Polega ona na wprowadzeniu rozpylonego oleju z dodatkiem katalizatora do reaktora zawierającego wodór.
           Przemysł metalurgiczny
W przemyśle metalurgicznym wodór używany jest do redukcji rudy żelaza. Wodór wykorzystywany jest w mieszaninie z tlenkiem węgla, który jest źródłem węgla potrzebnym do produkcji stali z surowego żelaza otrzymywanego w tym procesie. Przykładami reakcji redukcji rud żelaza są:
   
Termin „ekonomia wodoru”, który odnosi się do ekonomicznych aspektów stosowania wodoru jako źródła energii, został po raz pierwszy użyty podczas dyskusji w General Motors w 1970 roku. Został on spopularyzowany na przełomie XX i XXI wieku, gdy prace nad wykorzystaniem wodoru jako źródła energii przybrały na sile, kiedy szereg państw włączył się w rozwój technologii mających na celu ograniczenie emisji dwutlenku węgla. Do działań tych państwa zobowiązały się na konferencji w Kioto w 1997 roku.
--> Wodór jako paliwo konwencjonalne – pojęcie stosowane w odniesieniu do funkcji wodoru jako nośnika energii uwalnianej pod wpływem procesu spalania (w przeciwieństwie do np. procesu łączenia wodoru i tlenu w ogniwach paliwowych).
Charakterystyka
Wodór ma największą z paliw wartość opałową i ciepło spalania (w odniesieniu do masy). Ze względu na bardzo małą gęstość, wodór niekorzystnie prezentuje się na tle innych paliw, jeżeli wartości te zostaną odniesione do objętości. Z tego powodu wodór sprawdza się dobrze jako paliwo w przypadku pojazdów, w których masa odgrywa większą rolę niż objętość (np. rakietach lub statkach kosmicznych). Wodór ma bardzo wysoki współczynnik dyfuzji w azocie (który jest głównym składnikiem powietrza) co skutkuje dużą szybkością płomienia. Granice palności i wybuchowościwodoru przesunięte są silnie w kierunku końców skali, co skutkuje bardzo szerokim zakresem palności i wybuchowości mieszaniny wodoru i powietrza.

Historia: Pod koniec XVIII wieku rozpoczęła się w Europie rewolucja przemysłowa – szereg przemian, których konsekwencją było przejście od gospodarki opartej na rolnictwie i produkcji ręcznej do zautomatyzowanej produkcji przemysłowej (opierającej się głównie na mechanicznej produkcji fabrycznej na dużą skalę). Rozwój przemysłu, a w szczególności stosowanych w nim maszyn, spowodował że po początkowym okresie dominacji drewna jako paliwa zaczęto szukać nowych, bardziej wydajnych źródeł energii.
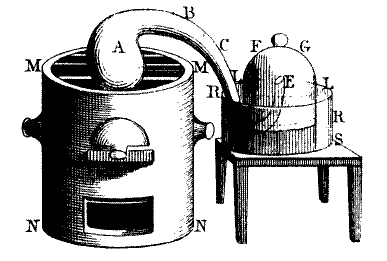
W 1783 Antoine Lavoisier odkrył, że łatwopalny gaz powstały w reakcji metali z kwasem siarkowym jest odrębnym pierwiastkiem. Hydrogenium, jak został nazwany, ze względu na swoje właściwości świetnie nadawał się na paliwo[2]. Część konstruktorów szybko dostrzegła jego zalety.
W 1807 szwajcarski konstruktor Isaac de Rivaz zbudował pierwszy pojazd kołowy napędzany silnikiem wodorowym. Silnik de Rivaza był jednym z pierwszych silników o spalaniu wewnętrznym [Silnik o spalaniu wewnętrznym to silnik, w którym paliwo spalane jest w przestrzeni roboczej silnika]. Centralny element silnika stanowił cylinder z komorą spalania [Komora spalania – element silnika cieplnego wykorzystującego wewnętrzne spalanie paliwajako sposób dostarczania górnego (dodatniego) ciepła obiegu termodynamicznego (silnik o spalaniu wewnętrznym). Spalanie paliwa następuje w sprężonym powietrzu lub w kontakcie z utleniaczem i może być realizowane w sposób ciągły (silniki turbinowe, rakietowe) lub cyklicznie (silniki tłokowe)], w której poruszał się tłok. Wybuchająca w komorze mieszanka wodoru i powietrza wprawiała tłok w ruch. W kolejnych latach de Rivaz udoskonalił swój pojazd. W 1813 ukończył budowę pojazdu, którego długość wynosiła 6 metrów, waga prawie tonę a każdy ruch cylindra przesuwał pojazd o cztery do sześciu metrów.

Pojazd de Rivaza
François Isaac de Rivaz (ur. 19 grudnia 1752 w Paryżu – zm. 30 lipca 1828 w Sion w Szwajcarii) - szwajcarski wynalazca, twórca pierwszego działającego silnika spalinowego dwusuwowego. Rivaza zainspirował idea silnika, zaproponowana przez Holendra Christiaana Huygensa, który jednak swojego pomysłu nie zrealizował oraz pomysł Philippe Lebona, który opracował tłok poruszany przez energię spalanego gazu. Silnik Rivaza zasilany był mieszanką wodoru i tlenu, opracowany został w 1806 roku. Konstrukcja nie była trwała, gdyż nie był wówczas dostępny materiał, w którym można byłoby prowadzić reakcję spalania. W rok później Rivaz skonstruował jednak pojazd napędzany swoim silnikiem i rozwijał go aż do wersji finalnej z 1813 roku.
     
(...) W 1820 William Cecil opublikował traktat On the Application of Hydrogen Gas to produce a moving Power in Machinery, w którym opisał zalety silnika napędzanego wodorem.

 
W literaturze: Zalety wodoru dostrzegli nie tylko sami konstruktorzy i inżynierowie, ale również wizjonerzy. W 1874 r. francuski pisarz Juliusz Verne, powszechnie uważany za jednego z protoplastów fantastyki naukowej, wydał książkę Tajemnicza wyspa, w której zawarł wizję wodoru jako źródła energii, które w przyszłości zdominuje technikę. Wizja Verne'a miała wpływ na przyszłych badaczy.
       
zwana była też "The Martians" (Marsjanie).
W roku 1963 Wigner otrzymał, razem z Hansem Jensenem i Marią Goeppert-Mayer, nagrodę Nobla w dziedzinie fizyki.
*Dr Hillard Bell Huntington (21 grudnia 1910 w Wilkes Barre , Luzerne County, Pensylwania - 17 lipca 1992 r. Troy , Rensselaer County, Nowy Jork) był fizykiem, który (wraz z Eugene'em Wignerem ) po raz pierwszy zaproponował, w 1935 r., Że wodór może wystąpić w stan metaliczny . [1] Znany jest również z pracy nad elektromagnezacją atomów, która później stała się ważnym zagadnieniem w elektronice półprzewodnikowej.

Huntington urodził się w Wilkes Barre w Pensylwanii i otrzymał tytuł licencjata (1932), magistra (1933) i doktora (1941) na Uniwersytecie Princeton . [2] Uczył w Culver Military Academy , University of Pennsylvania i Washington University w St. Louis. Podczas II wojny światowej Huntington pracował w Laboratorium Radiacyjnym na MIT.
Huntington dołączył do wydziału Rensselaer Polytechnic Institute w 1946 roku. Był przewodniczącym wydziału fizyki w RPI w latach 1961-1968. Był znany jako specjalista od procesów dyfuzji i przewodzenia w metalach. [2] Ivar Giaever , który zdobył nagrodę Nobla w dziedzinie fizyki w 1973 roku, był jednym z jego uczniów. [3] Był także znakomitym malarzem. [2] Niektóre z jego obrazów można znaleźć w bibliotece Hillarda B. Huntingtona ("HBH"), nazwanej na jego cześć, znajdującej się w centrum naukowym Jonsson-Rowland w RPI. RPI ustanowiło także nagrodę Hillarda B. Huntingtona dla absolwentów na jego cześć.
  Serie widmowe
Wodór ma charakterystyczne serie widmowe:
 
Skok Lymana – to nagły spadek natężenia widma ciągłegoatomu wodoru na granicy serii Lymana, zachodzący na długości fali 91,18 nm (911,8 Å).
Granica ta odpowiada punktowi zaabsorbowania energii, w którym elektrony pierwotnie znajdujące się na orbitalu 1 (seria K) zostają jonizowane.
                     
Biowodór - rodzaj biopaliwa. Od zwykłego wodoru odróżnia go sposób produkcji w procesie biologicznym lub biologiczno-chemicznym z biomasy lub bezpośrednio z fotosyntetycznego rozkładu wody.
Biowodór może być wytwarzany przez chemiczne przemiany biomasy (np. zgazowanie), konwersję biogazu: CH4 + H2O → CO + 3H2, niektóre rodzaje fermentacji anaerobowych, np. przez Clostridium acetobutilicum, Clostridium butyricum, Rhodobacter sphaeroides, Enterobacter cloacae, a także w nietypowej fotosyntezie przez hydrogenazę jak to czyni Chlamydomonas reinhardtii.
*Przechowywanie wodoru – dział techniki poświęcony metodom przechowywania wodoru, głównie jako paliwa o bardzo wysokiej wartości energetycznej. Przechowywanie wodoru jest przedmiotem licznych badań, zarówno cywilnych jak i wojskowych, ośrodków naukowych, szczególnie w kontekście zwiększonego zainteresowania bezpieczeństwem energetycznym i polityką ochrony środowiska naturalnego przed szkodliwymi skutkami użytkowania paliw kopalnych. Atrakcyjność wodoru jako źródła energii wynika z tego, że można go stosunkowo łatwo pozyskiwać z gazu ziemnego oraz wody, która jest też jedynym produktem jego spalania lub utleniania tlenem.
Spis treści
Wodór jest wytwarzany na skalę przemysłową w kilku procesach, z których najbardziej korzystnym ekonomicznie jest wytwarzanie wodoru z gazu ziemnego i gazów towarzyszących ropie naftowej (reforming parowy). Wodór jest również wytwarzany na drodze elektrolizy wody, co pozwala na uzyskanie wodoru o dużej czystości (około 99,9%).
Skroplony wodór od lat 40. XX wieku stosuje się w silnikach rakietowych, które wykorzystują energię odrzutu gazów powstającą przy spalaniu paliwa zmieszanego z utleniaczem (ciekłym tlenem). Wodór może być również spalany w klasycznym silniku tłokowym[1]. Szerokie zastosowanie znajdują ogniwa paliwowe zasilane wodorem, służące jako źródło energii elektrycznej zarówno dla urządzeń elektronicznych, jak i pojazdów mechanicznych[2].,[3] Wodór może zatem być traktowany jako bezpośrednie źródło energii lub jako, alternatywny dla ogniw galwanicznych, sposób magazynowania energii uzyskanej z innych źródeł (na przykład energii wiatru).
Wodór w normalnych warunkach jest gazem, więc jego objętościowa gęstość energii jest niewielka w porównaniu do ciekłych paliw kopalnych. Oznacza to, że dla dostarczenia jednakowej ilości energii potrzebna jest o wiele większa objętość wodoru (a zatem zbiornik o większej objętości) niż w przypadku paliw płynnych, na przykład benzyny. Stosowane są różnorodne metody przechowywania wodoru w postaci gazowej i ciekłej. Najnowsze podejście do tego zagadnienia zakłada przechowywanie wodoru związanego na drodze chemisorpcji lub fizysorpcji (lub obydwu jednocześnie) w materiałach stałych. Przechowywanie wodoru w materiałach stałych jest najbardziej korzystne zarówno ze względu na bezpieczeństwo użycia wodoru, jak i ze względów energetycznych (znacznie zwiększona gęstość objętościowa energii).
        
*Biekscyton (molekuła ekscytonowa) – kwazicząstka powstała jako stan związany dwóch ekscytonów.
Zachodzi analogia pomiędzy biekscytonem a cząsteczką wodoru (H2). Energia biekscytonu jest mniejsza niż suma energii tworzących go ekscytonów, analogicznie jak energia ekscytonu jest mniejsza niż suma energii tworzących go elektronu i dziury. Gęstość stanów biekscytonu w funkcji mocy pobudzającej zmienia się kwadratowo, w przeciwieństwie do ekscytonu gdzie zależność jest liniowa.
*Choroba wodorowa miedzi – szkodliwe zjawisko zachodzące w miedzi. Powyżej temperatury 380 °C tlen w miedzi występuje w postaci tlenku miedzi(I) Cu2O (poniżej znajduje się w postaci tlenku miedzi(II) CuO). Wskutek wyżarzania w temperaturze powyżej 500 °C następuje dyfuzja atomów wodoru w głąb sieci krystalicznej tego metalu. Atomy wodoru potrafią penetrować miedź na znaczne głębokości. Wodór w miedzi reaguje z zawartym w niej tlenkiem miedzi, w której to reakcji wydziela się para wodna:
Para wodna, która nie będąc w stanie wydostać się na zewnątrz, gromadzi się wewnątrz struktury krystalicznej, wytwarzając znaczne ciśnienie, które powoduje powstawanie mikropęknięć i naderwań oraz zmniejszenia plastyczności miedzi.
Choroby wodorowej można uniknąć poprzez użycie miedzi niezawierającej tlenu lub przez wyżarzanie w atmosferze niezawierającej wodoru i jego łatwo rozkładających się związków.
*Wodorowe zużycie metalu – zjawisko łuszczenia się współpracujących powierzchni metali na skutek wnikania w wysokiej temperaturze wodoru w strukturę tych powierzchni. Prowadzi to do nieodwracalnych zmian, które zdecydowanie przyśpieszają proces niszczenia metali. Efektem jest zniszczenie warstwy wierzchniej oraz tzw. zmęczenie materiału.
Współtwórcą techniki "blokowania mechanizmu wodorowego zużycia" metali jest George P. Shpenkov[1] - były członek Amerykańskiego Stowarzyszenia Trybologów.
*Stały wodór – pierwiastkowy wodór w stałym stanie skupienia.
Stały wodór powstaje z ciekłego wodoru poniżej jego temperatury krzepnięcia, czyli 14,01 K (−259,14 °C). Po raz pierwszy został otrzymany w 1899 roku przez Jamesa Dewara[1].
Objętość molowa stałego wodoru wynosi 22,7 cm³/mol, co odpowiada gęstości 0,088 g/cm3[2]. Dla izotopów wodoru, deuteru i trytu, gęstości wynoszą odpowiednio 0,20 i 0,31 g/cm3.
 
*Mezonium – odmiana atomu wodoru, w którym jądro atomowe stanowi dodatnio naładowany mezon (np. kaon, pion), a nie proton.
Badanie takich obiektów służy weryfikowaniu przewidywań fizyki, głównie kwantowej.
*Mionium (symbol Mu) – nazwa egzotycznego atomuzbudowanego z antymionu i elektronu (μ+ i e–)[1]. Mionium strukturą przypomina atom wodoru; antymion, którego masa jest 207 razy większa od elektronu[2], zajmuje w nim miejsce protonu. Ze względu na dużą różnicę mas cząstek mionium przypomina atom wodoru także pod względem energii jonizacji i promienia atomu w modelu Bohra. Stan podstawowy mionium ma energię -13,54 eV, bardzo bliską wartości -13,64 eV dla wodoru[3].
Mionium jest nietrwałe ze względu na rozpad antymionu na pozyton i dwa neutrina. Jego średni czas życia to 2,2 mikrosekundy. Jest on wystarczająco długi, żeby mionium było w stanie wchodzić w reakcje chemiczne i obecnie znanych jest kilka jego związków; pod względem chemicznym zachowuje się ono jak promieniotwórczyizotop wodoru[4]. Do znanych związków należą:
*Atom egzotyczny – atom, w którym jedna lub więcej cząstek zostały zastąpione innymi cząstkami o tym samym ładunku. Na przykład atomy mionowe i atomy hadronowe to atomy, w których elektron jest zastąpiony inną ujemną cząstką. Do atomów egzotycznych należą również takie, w których jądro zastąpione jest inną cząstką dodatnią, na przykład pozytonium (elektron i pozyton), mionium (elektron i dodatni mion) oraz pionium (pion i mion), a także atomy z hiperjądrem.
Atomy mionowe
Atom mionowy to atom egzotyczny, w którym elektron (lub elektrony) jest zastąpiony mionem. Mion, podobnie jak elektron, jest leptonem.
Atomy hadronowe
Atomy egzotyczne, w których elektron jest zastąpiony ujemnym hadronem. Należą do nich mezoatomy (elektron zastąpiony mezonem, na przykład pionem lub kaonem (również mionem)[1]), protonium (elektron zastąpiony antyprotonem) oraz hiperatomy (elektron zastąpiony ujemnym hiperonem[2], np. Σ- – atomy sigmowe).
Atomy pionowe zostały odkryte w 1952, kaonowe w 1960, sigmowe w 1968, a antyprotonowe w 1970.
Atomy hadronowe otrzymuje się przez kierowanie wiązki ujemnych hiperonów z akceleratora na tarczę z odpowiedniego materiału, np. potasu, cynku lub ołowiu. Ich czas życia jest rzędu 10−12 s.
Badanie nad mezoatomami pokazały, że mion jest leptonem, a nie hadronem[1].
Atomy z hiperjądrem
Atomy (również nazywane hiperatomami[3]) mogą też składać się z elektronów krążących wokół hiperjądra, czyli jądra, w którym co najmniej jeden nukleon został zastąpiony hiperonem.
| |||||||||||||||

































































































Brak komentarzy:
Prześlij komentarz