Helowce (Gazy szlachetne) - są to pierwiastki chemiczne ostatniej, 18 (daw. 0 lub VIII głównej) grupy układu okresowego. Do pierwiastków tych zalicza się hel, neon, argon, krypton, ksenon i radon. Prawdopodobnie gazem szlachetnym jest również syntetyczny pierwiastek oganesson.
Właściwości: Wszystkie helowce są bezbarwnymi, bezwonnymi, słabo rozpuszczającymi się w wodzie gazami. Mają niskie temperatury topnienia.
*Pod ciśnieniem normalnym.
**Hel pod normalnym ciśnieniem nie przechodzi w stan stały nawet w najniższej osiągalnej temperaturze.
***Najtrwalszy znany izotop.
**Hel pod normalnym ciśnieniem nie przechodzi w stan stały nawet w najniższej osiągalnej temperaturze.
***Najtrwalszy znany izotop.
Pierwiastki te są wysoce niereaktywne. Wynika to z faktu, że nie zawierają one żadnych częściowo zapełnionych elektronami orbitali, które mogłyby uczestniczyć w tworzeniu wiązań chemicznych. W dół grupy powoli zwiększa się reaktywność tych pierwiastków. Spowodowane jest to tym, że zwiększa się ich rozmiar, a z nim odległość elektronów walencyjnych od środka jądra.
Pomimo bardzo niskiej reaktywności lżejszych helowców, znane są nietrwałe związki helu: cząsteczka He2, jon HeH+ i LiHe. Na przełomie 2016/2017 doniesiono o otrzymaniu pierwszego stałego związku helu, Na2He, który jest trwały termodynamicznie pod ciśnieniem powyżej 113 GPa (ok. 1,1×106 atm). Tworzy kryształy o strukturze fluorytu.
Znany jest też związek argonu – fluorowodorek argonu, otrzymany w temperaturze około 40 K.
Krypton i ksenon tworzą większą liczbę związków, lecz są one często trudne do uzyskania i niekiedy nietrwałe w temperaturze poojowej. Działając ksenonem na heksafluorek platyny Neil Bartlett (opierając się na wcześniejszym odkryciu wraz z Lohmannem heksafluoroplatynianu dioksygenylu) otrzymał trwały czerwonopomarańczowy związek, heksafluoroplatynian ksenonu.
(...) Stosunkowo najbardziej reaktywny jest radon. Istnieje trwały chemicznie związek - fluorek radonu RnF2. Powstaje on z mieszaniny fluoru i radonu w temperaturze ok. 400 stopni Celsjusza. Cząstka ta rozpada się jednak ze względu na radioaktywność radonu.
(...) Hel, neon, argon i ksenon występują w niewielkich ilościach w powietrzu i dlatego podstawowym sposobem ich otrzymywania jest destylacja frakcyjna powietrza. Krypton i radon są produktami rozpadu promieniotwórczego uranu i toru i towarzyszą zwykle złożom rud tych metali, dzięki czemu można te złoża stosunkowo łatwo wykrywać.
Gazy szlachetne w niskich temperaturach tworzą kryształy związane słabymi oddziaływaniami van der Waalsa. Hel przy zerowym ciśnieniu nie krystalizuje nawet w temperaturach bliskich 0 K; dominującą rolę odgrywa tu energia drgań zerowych, która destabilizuje kryształ. Drgania zerowe powodują też zmniejszenie wartości energii kohezji kryształów w porównaniu z sumaryczną energią oddziaływań van der Waalsa.
Ze względu na zależność energii drgań zerowych od masy to zmniejszenie jest tym większe, im mniejsza jest masa atomu (np. dla neonu zmniejsza ją o wartość 28%, a dla ksenonu – o 4%). Skutkuje to również różną wartością stałej sieci dla kryształów różnych izotopów danego gazu szlachetnego. Gazy szlachetne, z wyjątkiem helu, krystalizują w strukturze regularnej gęstego upakowania (fcc).
 Zastosowanie: Gazy szlachetne wykorzystuje się wszędzie tam, gdzie potrzebna jest obojętna, beztlenowa atmosfera zapobiegająca reakcjom utleniania. Stosuje się je do napełniania żarówek, do prowadzenia reakcji wymagających obojętnych warunków i do spieniania tworzyw sztucznych. Żaden z nich nie uczestniczy w procesach biologicznych, dlatego często używa się ich jako obojętnych gazów zapobiegających starzeniu się materiałów pochodzenia organicznego. Dla przykładu, oryginał Konstytucji oraz Deklaracji niepodległości Stanów Zjednoczonych przechowuje się w szczelnej gablocie wypełnionej helem.
Zastosowanie: Gazy szlachetne wykorzystuje się wszędzie tam, gdzie potrzebna jest obojętna, beztlenowa atmosfera zapobiegająca reakcjom utleniania. Stosuje się je do napełniania żarówek, do prowadzenia reakcji wymagających obojętnych warunków i do spieniania tworzyw sztucznych. Żaden z nich nie uczestniczy w procesach biologicznych, dlatego często używa się ich jako obojętnych gazów zapobiegających starzeniu się materiałów pochodzenia organicznego. Dla przykładu, oryginał Konstytucji oraz Deklaracji niepodległości Stanów Zjednoczonych przechowuje się w szczelnej gablocie wypełnionej helem. 1) Hel (He, łac. Helium) - jest to pierwiastek chemiczny o liczbie atomowej 2, z grupy helowców (gazów szlachetnych) w układzie okresowym. Jest po wodorze drugim najbardziej rozpowszechnionym pierwiastkiem chemicznym we wszechświecie , jednak na Ziemiwystępuje wyłącznie w śladowych ilościach (4×10−7% w górnych warstwach atmosfery).
1) Hel (He, łac. Helium) - jest to pierwiastek chemiczny o liczbie atomowej 2, z grupy helowców (gazów szlachetnych) w układzie okresowym. Jest po wodorze drugim najbardziej rozpowszechnionym pierwiastkiem chemicznym we wszechświecie , jednak na Ziemiwystępuje wyłącznie w śladowych ilościach (4×10−7% w górnych warstwach atmosfery).
Hel na Ziemi występuje głównie w atmosferze(5,2×10−4% obj. w powietrzu), pochodzi głównie z rozpadu jąder promieniotwórczych w naturalnych szeregach promieniotwórczych. W litosferze hel występuje również w niektórych złożach gazu ziemnego. W gazach występujących w Stanach Zjednoczonychdochodzi do 1%, w gazach występujących w Europieilość ta jest bardzo mała (z wyjątkiem Polski – do 3%). Praktycznie cały hel, który mógł pierwotnie istnieć na Ziemi, nie mogąc związać się z żadnym innym pierwiastkiem, jako bardzo lekki opuścił atmosferę Ziemi.
Występuje w postaci dwóch izotopów trwałych – 3He i 4He. Znanych jest także kilka syntetycznych izotopów nietrwałych (T½ < 1 sekundy), z których najbardziej stabilne są 6He i 8He.
Hel jest najmniej aktywnym pierwiastkiem chemicznym, z najwyższą spośród wszystkich pierwiastków energią jonizacji (24,59 eV). Znane są jego związki metastabilne (np. HHeF, (HeO)(CsF) i LiHe) i krótko żyjące cząsteczki HeNe i jony He+ oraz He2+. Tworzy też stabilne stałe związki międzycząsteczkowe, np. NeHe2 i He@H2O. Na przełomie 2016/2017 doniesiono o otrzymaniu pierwszego stałego związku helu, Na2He, który jest trwały termodynamicznie pod ciśnieniem powyżej 113 GPa (ok. 1,1×106 atm). Tworzy kryształy o strukturze fluorytu. Nie ma żadnego znaczenia biologicznego.
Odkrycie helu: Hel odkryto najpierw na Słońcu, później na Ziemi. Podczas całkowitego zaćmienia Słońca, które miało miejsce 18 sierpnia 1868 roku i było widoczne w Indiach, astronom Pierre Janssen, badając widmo korony słonecznej, zaobserwował pomarańczowy prążek odpowiadający długości fali 587,6 nm, którego nie można było przypisać do żadnego spośród znanych wówczas pierwiastków. Ten sam prążek w widmie Słońca zaobserwował 20 października 1868 r. angielski astronom Norman Lockyer. Lockyer i angielski chemik Edward Frankland nadali nowemu pierwiastkowi – emitującemu falę o długości 587,6 nm – nazwę helium od greckiego boga słońca – Heliosa. Przez wiele lat hel był uważany za pierwiastek, który występuje na Słońcu, ale nie występuje na Ziemi. W roku 1895 William Ramsay otrzymał hel po potraktowaniu kleweitu (rudy uranowej) kwasem mineralnym. Ramsay przesłał próbkę gazu do Williama Crookesa i Normana Lockyera, którzy zidentyfikowali hel.
(...)
Hel stały: Hel jako jedyny pierwiastek pozostaje ciekły nawet w temperaturze zera bezwzględnego (pod ciśnieniem atmosferycznym) i zestala się dopiero w podwyższonym ciśnieniu. Ma najniższą temperaturę krzepnięcia spośród wszystkich pierwiastków: <0,95 K (pod ciśnieniem 26 atm). W zależności od ciśnienia hel w stanie stałym może zmieniać objętość o 30%. W temperaturze poniżej 0,2–0,4 K hel stały przechodzi przemianę fazową do formy o właściwościach nadciekłych ("hel nadstały").
- Zero bezwzględne (temperatura zera bezwzględnego, zero absolutne) – temperatura równa zero w termodynamicznej skali temperatur, czyli jest to temperatura, w której wszystkie elementy układu termodynamicznego uzyskują najniższą z możliwych energii. Temperatura ta odpowiada −273,15 °C = 0 K.

-
-
 6) Radon (Rn, łac. Radon) - jest to pierwiastek chemiczny z grupy gazów szlachetnych w układzie okresowym. Został odkryty w 1900 roku przez Friedricha Dorna. Początkowo nazywany był "emanacją" (symbo: Em), proponowano dla niego także nazwę "niton" (Nt). Niektóre jego izotopy nosiły własne nazwy, pochodzące od pierwiastków z których powstały, jak 222Rn – „radon”, 220Rn – „toron” (symbol Tn) lub 219Rn – „aktynon” (An). Dopiero po roku 1923 przyjęto jako obowiązującą nazwę najtrwalszego izotopu.
6) Radon (Rn, łac. Radon) - jest to pierwiastek chemiczny z grupy gazów szlachetnych w układzie okresowym. Został odkryty w 1900 roku przez Friedricha Dorna. Początkowo nazywany był "emanacją" (symbo: Em), proponowano dla niego także nazwę "niton" (Nt). Niektóre jego izotopy nosiły własne nazwy, pochodzące od pierwiastków z których powstały, jak 222Rn – „radon”, 220Rn – „toron” (symbol Tn) lub 219Rn – „aktynon” (An). Dopiero po roku 1923 przyjęto jako obowiązującą nazwę najtrwalszego izotopu.
-
- łac. emano = wypływam
- (...) Właściwości fizyczne: Radon jest bezbarwnym, bezwonnym radioaktywnym gazem szlachetnym. Występuje naturalnie, jako produkt rozpadu radu, który z kolei powstaje z obecnego w przyrodzie w sporych ilościach uranu. Jego najstabilniejszy izotop 222Rn ma okres połowicznego rozpadu 3,8 dnia i jest stosowany w radioterapii. Gęstość radonu wynosi 9,73 kg/m³ – jest on 8 razy cięższy niż średnia gęstość gazów atmosferycznych. W temperaturze pokojowej jest bezbarwny, ale schłodzony do punktu zamarzania (−71 °C), nabiera barwy żółtej, a poniżej −180 °C staje się pomarańczowo-czerwony. Emituje również intensywną poświatę, będącą efektem jego radioaktywności.
Promieniotwórczość: Radon w czasie rozpadu emituje promieniowanie alfa (oraz w mniejszym stopniu beta) o małej przenikliwości, ale o dużej zdolności jonizującej (wysoka energia, duża masa cząstki). 222Rn jest izotopem naturalnym, pochodzącym bezpośrednio z rozpadu 226Ra (o okresie połowicznego zaniku 1600 lat). Ten ostatni z kolei jest długożyciowym produktem przemian radioaktywnych zachodzących w naturalnym szeregu promieniotwórczym, którego pierwszym członem jest naturalny izotop uranu 238U. Zawartość uranu w skorupie ziemskiej wynosi średnio 2 ppm (0,0002%), więc stosunkowo dużo. Dlatego też zawartość 222Rn w powietrzu atmosferycznym w warstwie przypowierzchniowej jest znacząca. Średnie stężenie 222Rn w powietrzu w Polsce wynosi ok. 10 Bq/m³. Promieniowanie pochodzące od radonu stanowi 40–50% dawki promieniowania, jaką otrzymuje mieszkaniec Polski od źródeł naturalnych. Radon może stanowić zagrożenie dla zdrowia człowieka, bowiem gromadzi się w budynkach mieszkalnych, zwłaszcza w piwnicach, przedostając się tam z gruntu w wyniku różnicy ciśnień (efekt kominowy). Dotyczy to zwłaszcza podłoża granitowego, zawierającego większe ilości uranu w swoim składzie niż np. skały osadowe. Aktualnie w Polsce obowiązuje limit stężenia radonu w nowych budynkach mieszkalnych wynoszący 200 Bq/m³[6]. Szkodliwość radonu jest wynikiem stosunkowo szybkiego jego rozpadu, prowadzącego do powstania kilku krótkożyciowych pochodnych, również radioaktywnych, emitujących promieniowania alfa. Ich zatrzymanie w płucach będzie powodować uszkodzenia radiacyjne, prowadzące do rozwoju choroby nowotworowej.
(...) Radon a zdrowie: Radon jest pierwiastkiem stosowanym w medycynie – naturalnie występujące wody radonowe stosuje się do kąpieli w rehabilitacji chorób narządów ruchu, zarówno tych pourazowych, jak i reumatycznych. Kąpiele radonowe stosowane są też do leczenia cukrzycy, chorób stawów, chorób tarczycy oraz schorzeń ginekologicznych i andrologicznych. Przedawkowanie radonu lub stała praca przy kopalinach, gdzie są silne emanacje radonu, wpływa niekorzystnie na zdrowie. Szkodliwe efekty działania radonu polegają na uszkadzaniu struktury chemicznej kwasu DNA przez wysokoenergetyczne, krótkotrwałe produkty rozpadu radonu 222Rn, co może powodować chorobę popromienną.
(...)
Właściwości chemiczne radonu: Właściwości radonu są stosunkowo słabo znane, ze względu na jego wysoką radioaktywność. Radon należy do grupy gazów szlachetnych, które z definicji powinny być chemicznie obojętne. Mimo to znanych jest kilka jego związków na różnych stopniach utlenienia. Są to m.in. fluorki RnF2, RnF4, RnF6, chlorek RnCl4 i tritlenek radonu RnO3. Ze względu na nietrwałość samego radonu nie mają one żadnych zastosowań.
Izotopy radonu: Naturalnie występują cztery izotopy radonu, które powstają w wyniku rozpadu uranu 238U (218Rn i 222Rn), 235U (219Rn) i toru 232Th (220Rn). Spośród nich izotop 222Rn ma zdecydowanie najdłuższy czas trwania – 3,8 dnia (pozostałe <1 dzień). Stanowi on praktycznie 100% radonu spotykanego naturalnie i ma możliwość migracji i gromadzenia się. Oprócz występujących naturalnie izotopów, znanych jest około 30 innych wytworzonych sztucznie w laboratorium.
| Izotop | Okres połowicznego rozpadu |
|---|---|
| 195Rn | 6 ms |
| 196Rn | 4,7 ms |
| 197Rn | 66 ms |
| 198Rn | 65 ms |
| 199Rn | 620 ms |
| 200Rn | 0,96 s |
| 201Rn | 7,0 s |
| 202Rn | 9,94 s |
| 203Rn | 44,2 s |
| 204Rn | 1,17 min |
| 205Rn | 170 s |
| 206Rn | 5,67 min |
| 207Rn | 9,25 min |
| 208Rn | 24,35 min |
| 209Rn | 28,5 min |
| 210Rn | 2,4 h |
| 211Rn | 14,6 h |
| 212Rn | 23,9 min |
| 213Rn | 19,5 ms |
| 214Rn | 0,27 µs |
| 215Rn | 2,30 µs |
| 216Rn | 45 µs |
| 217Rn | 0,54 ms |
| 218Rn | 35 ms |
| 219Rn | 3,96 s |
| 220Rn | 55,6 s |
| 221Rn | 25,7 min |
| 222Rn | 3,8235 dni |
| 223Rn | 24,3 min |
| 224Rn | 107 min |
| 225Rn | 4,66 min |
| 226Rn | 7,4 min |
| 227Rn | 20,8 s |
| 228Rn | 65 s |
Naukowcy skupieni wokół Klausa Blauma z Instytutu Fizyki Jądrowej im. Maksa Plancka w Heidelbergu i Lutza Schweikharda z Uniwersytetu w Greifswald odkryli nowy izotop radonu 229Rn. Niestabilny nuklid odkryto dzięki innowacyjnej metodzie wysokoprecyzyjnej spektrometrii masowej w pułapce Penninga. Po raz pierwszy określono również masę jąder sześciu innych bogatych w neutrony izotopów radonu.
Tabela nuklidów jest dla fizyków jądrowych tym, czym dla chemików układ okresowy pierwiastków. Przedstawione są na niej wszystkie znane jądra atomowe (nuklidy), uporządkowane według liczby protonów i neutronów. Do 3175 odkrytych dotychczas rodzajów jąder dołączył niedawno kolejny rodzaj — nowy izotop radonu składa się z 86 protonów i 143 neutronów. Radon to radioaktywny gaz szlachetny, którego najtrwalszym izotopem jest izotop o liczbie masowej 222, którego okres połowicznego rozpadu wynosi prawie cztery dni, a powstaje on wskutek rozpadu izotopu radu 226Ra. Okres połowicznego rozpadu nowego izotopu wynosi natomiast zaledwie 12 sekund.
Najbardziej godnym uwagi jest to, że po raz pierwszy międzynarodowemu zespołowi naukowców udało się bezpośrednio dowieść istnienia nowego izotopu za pomocą jego zamknięcia w specjalnej pułapce dla jonów, zwaną pułapką Penninga. Urządzenie to służy do przechowywania przez dłuższy czas pojedynczych jonów, a następnie do precyzyjnych pomiarów ich mas. W ten sposób masa nowego izotopu, a także masy izotopów sąsiednich o liczbach masowych od 223 do 228 mogły zostać określone z dokładnością do kilku milionowych procenta.
Takie nie występujące w środowisku naturalnym jądra wyprodukowano w laboratorium izotopowym ISOLDE Europejskiej Organizacji Badań Jądrowych CERN na drodze bombardowania jądra uranu wysokoenergetycznymi protonami.
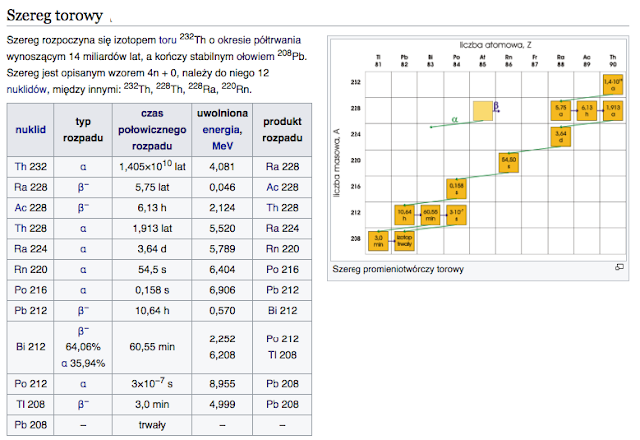
Na ilustracji przedstawiony został fragment tablicy nuklidów dla pierwiastków pomiędzy ołowiem a radem. Stabilne nuklidy zabarwione są na czarno, kolorami oznaczono proces rozpadu radioaktywnych nuklidów: jasnoniebieski i różowy – rozpad alfa, żółty – rozpad beta. W tabeli wyróżnione zostały naturalne nuklidy 208Pb, 222Rn, 226Ra, a także nowoodkryty 229Rn (z prawej). W prawym górnym rogu - pułapka Penninga. JSL
Najbardziej godnym uwagi jest to, że po raz pierwszy międzynarodowemu zespołowi naukowców udało się bezpośrednio dowieść istnienia nowego izotopu za pomocą jego zamknięcia w specjalnej pułapce dla jonów, zwaną pułapką Penninga. Urządzenie to służy do przechowywania przez dłuższy czas pojedynczych jonów, a następnie do precyzyjnych pomiarów ich mas. W ten sposób masa nowego izotopu, a także masy izotopów sąsiednich o liczbach masowych od 223 do 228 mogły zostać określone z dokładnością do kilku milionowych procenta.
Takie nie występujące w środowisku naturalnym jądra wyprodukowano w laboratorium izotopowym ISOLDE Europejskiej Organizacji Badań Jądrowych CERN na drodze bombardowania jądra uranu wysokoenergetycznymi protonami.

Na ilustracji przedstawiony został fragment tablicy nuklidów dla pierwiastków pomiędzy ołowiem a radem. Stabilne nuklidy zabarwione są na czarno, kolorami oznaczono proces rozpadu radioaktywnych nuklidów: jasnoniebieski i różowy – rozpad alfa, żółty – rozpad beta. W tabeli wyróżnione zostały naturalne nuklidy 208Pb, 222Rn, 226Ra, a także nowoodkryty 229Rn (z prawej). W prawym górnym rogu - pułapka Penninga. JSL
Źródło: focus.pl
*Wody radonowe – wody mineralne zawierające niewielkie ilości nietrwałego pierwiastka promieniotwórczego radonu i produkty jego rozpadu promieniotwórczego. W Polsce zalicza się do nich te wody, które wykazują aktywność promieniotwórczą co najmniej 74 Bq/l (2 nCi/l). Podstawą racjonalności leczniczego efektu wód radonowych jest hipoteza hormezy radiacyjnej. Natomiast zdaniem zwolenników liniowego modelu bezprogowego (LNT, z ang. Linear No-Threshold) szkodliwa jest nawet najmniejsza dawka promieniowania jonizującego.
ZWIĄZKI RADONU:
 7) Oganesson (Og) - jest to niewystępujący naturalnie na Ziemi pierwiastek chemiczny z grupy transaktynowców o liczbie atomowej 118. Został otrzymany po raz pierwszy w 2002 roku w Zjednoczonym Instytucie Badań Jądrowych (JINR) w Dubnej w Rosji przez zespół rosyjskich i amerykańskich naukowców. Odkrycie zostało zatwierdzone przez IUPAC i IUPAP w 2015 roku, a w roku 2016 nowemu pierwiastkowi nadano nazwę oganesson. Nazwa ta honoruje rosyjskiego fizyka jądrowego, Jurija Oganiesiana, który odegrał wiodącą role w odkryciu najcięższych pierwiastkó∑ układu okresowego i był kierownikiem zespołu, który dokonał syntezy oganessonu. Był to drugi (po seaborgu) przypadek nazwania pierwiastka na część osoby żyjącej.
7) Oganesson (Og) - jest to niewystępujący naturalnie na Ziemi pierwiastek chemiczny z grupy transaktynowców o liczbie atomowej 118. Został otrzymany po raz pierwszy w 2002 roku w Zjednoczonym Instytucie Badań Jądrowych (JINR) w Dubnej w Rosji przez zespół rosyjskich i amerykańskich naukowców. Odkrycie zostało zatwierdzone przez IUPAC i IUPAP w 2015 roku, a w roku 2016 nowemu pierwiastkowi nadano nazwę oganesson. Nazwa ta honoruje rosyjskiego fizyka jądrowego, Jurija Oganiesiana, który odegrał wiodącą role w odkryciu najcięższych pierwiastkó∑ układu okresowego i był kierownikiem zespołu, który dokonał syntezy oganessonu. Był to drugi (po seaborgu) przypadek nazwania pierwiastka na część osoby żyjącej.
(...) Oganesson jest wysoce niestabilny. W latach 2002–2005 udało się uzyskać jedynie 3 lub 4 atomy izotopu 294Og o czasie połowicznego rozpadu ocenianym na mniej niż 1 milisekunda. Nie pozwoliło to na eksperymentalne zbadanie jego właściwości chemicznych, jednak liczne są ich przewidywania na podstawie obliczeń teoretycznych. Jest on pierwszym sztucznym przedstawicielem 18 grupy układu okresowego, czyli gazów szlachetnych, i prawdopodobnie wykazuje największą spośród nich reaktywność chemiczną. W przeszłości sądzono, że oganesson w warunkach standardowych będzie gazem, jednak obecne przewidywania wskazują na stały stan skupienia w tych warunkach, wynikający z efektów relatywistycznych. W układzie okresowym leży w bloku p, będąc ostatnim pierwiastkiem siódmego okresu. W chwili pierwszej syntezy oganesson miał najwyższą liczbę atomową i największą masę atomową spośród wszystkich znanych pierwiastków.
Historia:
-> Pierwsze spekulacje: Duński fizyk Niels Bohr w 1922 rozrysował własną wersję układu okresowego, w którym umieścił pierwiastek 118 jako siódmy gaz szlachetny. W roku 1965 Aristid von Grosse opublikował swoje przewidywania dotyczące prawdopodobnych właściwości pierwiastka 118 na podstawie ekstrapolacji właściwości znanych pierwiastków. Pomimo że w tym czasie nie powstała jeszcze koncepcja wyspy stabilności, spekulacje von Grossego okazały się zgodne z późniejszymi obliczeniami. Rzeczywiste właściwości chemiczne oganessonunie zostały jeszcze zbadane i nie wiadomo, czy rzeczywiście zachowuje się jak gaz szlachetny.
-> Nieudane próby syntezy: Pod koniec 1998 polski fizyk Robert Smolańczuk opublikował obliczenia dotyczące fuzji jąder atomowych w celu otrzymywania superciężkich atomów, w tym przyszłego oganessonu. Jego wyliczenia sugerowały, że synteza tego pierwiastka może zostać przeprowadzona poprzez fuzję ołowiu i kryptonu w kontrolowanych warunkach.
W 1999 badacze w Lawrence Berkeley National Laboratory wykorzystali jego przewidywania i ogłosili odkrycie liwermoru oraz oganessonu w „Physical Review Letters”, po czym bardzo szybko wyniki zostały opisane w „Science”. Badacze stwierdzili, że udało im się przeprowadzić reakcję:
- 8636Kr + 20882Pb → 293118Og + 10n
Wkrótce jednak okazało się, że ani inne grupy naukowców, ani badacze samego laboratorium w Berkeley nie byli w stanie powtórzyć wyniku i po dwóch latach od publikacji doniesienie zostało wycofane przez autorów. W czerwcu 2002 dyrektor laboratorium ogłosił, że twierdzenie o odkryciu dwóch nowych pierwiastków oparte zostało na danych sfabrykowanych przez głównego autora, Wiktora Ninowa.
Potwierdzona synteza: W 2002 roku zespół naukowców rosyjskich ze Zjednoczonego Instytutu Badań Jądrowych w Dubnej, we współpracy z grupą amerykańską z Lawrence Livermore National Laboratory, pod kierownictwem fizyka jądrowego Jurija Oganiesiana, opublikował wstępny raport informujący o otrzymaniu pierwiastka 118. Pełen artykuł o udanej syntezie badacze przesłali do redakcji pisma Physical Review C 31 stycznia 2006 (ukazał się on 9 października 2006).
Otrzymali oni w sumie 3 (a być może 4) jądra oganessonu-294 (jedno lub dwa w 2002 i dwa kolejne w 2005). Otrzymano je przez zderzanie atomów kalifornu-249 z jonami wapnia-48:
24998Cf + 4820Ca → 294118Og + 310n
 Z powodu bardzo małego prawdopodobieństwa fuzji jądrowej(przekrój czynny wynosi około 0,3–0,6 pb, tj. (3–6)×10−41 m²), konieczne było długotrwałe bombardowanie próbki kalifornu strumieniem jonów wapnia – w ciągu 4 miesięcy trwania eksperymentu, w celu uzyskania jednego atomu pierwiastka 118, użyto ich 2,5×1019. Bombardowanie kontynuowano przez kolejne miesiące, uzyskując dwa następne atomy pierwiastka 118. Prawdopodobieństwo, że zaobserwowany wynik nie był związany z powstaniem pierwiastka 118, lecz wywołały go szumy lub zjawiska przypadkowe, oszacowano na mniej niż 1:100 000, wobec czego można było przyjąć z dużą pewnością, że rzeczywiście uzyskano oczekiwany pierwiastek.
Z powodu bardzo małego prawdopodobieństwa fuzji jądrowej(przekrój czynny wynosi około 0,3–0,6 pb, tj. (3–6)×10−41 m²), konieczne było długotrwałe bombardowanie próbki kalifornu strumieniem jonów wapnia – w ciągu 4 miesięcy trwania eksperymentu, w celu uzyskania jednego atomu pierwiastka 118, użyto ich 2,5×1019. Bombardowanie kontynuowano przez kolejne miesiące, uzyskując dwa następne atomy pierwiastka 118. Prawdopodobieństwo, że zaobserwowany wynik nie był związany z powstaniem pierwiastka 118, lecz wywołały go szumy lub zjawiska przypadkowe, oszacowano na mniej niż 1:100 000, wobec czego można było przyjąć z dużą pewnością, że rzeczywiście uzyskano oczekiwany pierwiastek.
W doświadczeniach tych zaobserwowano rozpad alfa 3 atomów. Zaproponowano również czwarty rozpad, będący spontanicznym rozpadem jądra. Czas połowicznego rozpadu obliczono na 0,89 ms. W wyniku emisji cząstki alfa z 294Og powstaje liwermor (290Lv). Jako że rozpadowi uległy jedynie 3 jądra atomowe, okres półtrwania wyliczony z ich obserwacji cechuje się znaczną niepewnością: 0,89 +1,07−0,31 ms[15]. W 2015 roku na podstawie danych zebranych dla większej liczby atomów czas połowicznego rozpadu 294Og wyznaczono na 0,7 ms.
*Nazwa 118 pierwiastka:































































































































































































Brak komentarzy:
Prześlij komentarz